Senyawa aromatik polisiklik lebih
reaktif terhadap serangan oksidasi, reduksi dan substitusi dibandingkan senyawa
benzena. Kereaktifan ini disebabkan kemampuan bereaksi dari suatu cincin,
sementara cincin lainnya masih dipertahankan.
1.
Reaksi Oksidasi
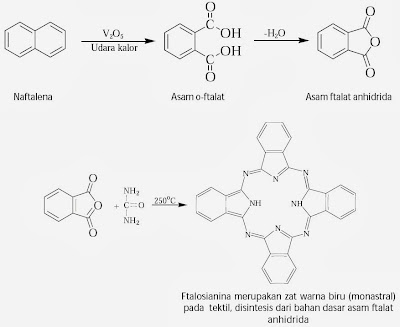
Asam
ftalat anhidrat dibuat dari oksidasi naftalena dengan katalis vanadium oksida. Persamaan
reaksinya :
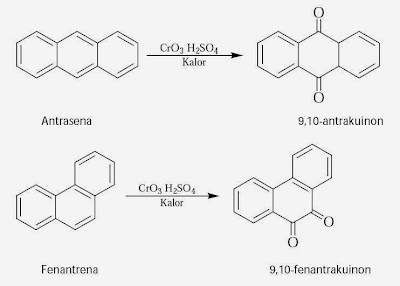
Antrasena dan
fetnantrena dapat juga dioksidasi menjadi suatu kuinon. Reaksinya :
2.
Reaksi Reduksi
Berbeda dari benzena, senyawa polisiklik dapat
dihidrogenasi (direduksi) parsial pada tekanan dan suhu kamar.
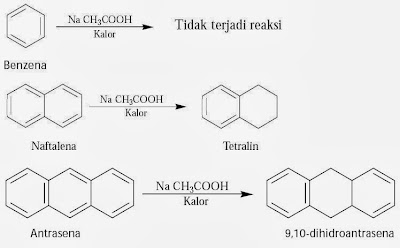
Perhatikan
bahwa system cincin yang tereduksi parsial masih mengandung cincin benzena. Sebagian
besar sifat aromatik dari system cincin masih ada dan dipertahankan.
Untuk
menghidrogenasi semua cincin aromatik dalam naftalena dapat dilakukan pada suhu
dan tekanan tinggi. Persamaan reaksinya :
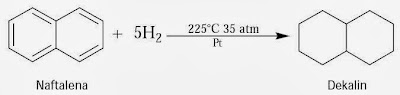
3.
Reaksi Substitusi
Semua cincin aromatik polisiklik lebih reaktif
terhadap serangan substitusi daripada benzena. Naftalena mengalamai reaksi substitusi
terutama pada posisi atom karbon nomor-1. Beberapa contoh reaksi substitusi aromatik
polisiklik di antaranya reaksi brominasi dan reaksi sulfonasi.
a.
Reaksi brominasi
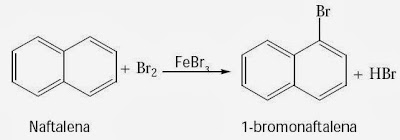
Berdasarkan
hasil percobaan diketahui bahwa naftalena dapat dibrominasi pada suhu kamar
menggunakan katalis FeBr3.
b.
Reaksi sulfonasi
Reaksi
sulfonasi pada naftalena dilakukan sama seperti pada benzena. Berdasarkan data
hasil percobaan diketahui bahwa reaksi sulfonasi naftalena dipengaruhi oleh
suhu.
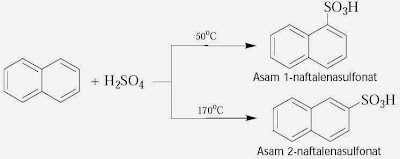
Pada
suhu dibawah 60oC, naftalena bereaksi dengan asam sulfat pekat membentuk
asam 1-naftalenasulfonat, tetapi pada suhu tinggi di atas 160oC,
menghasilkan campuran produk dari asam 2-naftalenasulfonat (85%) dan asam
1-naftalenasulfonat (15%).
yang ingin saya tanyakan adalah, bagaimana mekanisme terjadinya reaksi reduksi parsial pada naftalena?
BalasHapusNaftalena adalah salah satu komponen yang termasuk benzena aromatik hidrokarbon, tetapitidak termasuk polisiklik. Senyawa naftalen tidak sama seperti benzen. Senyawa polisiklik dapat dihidrogenasi (direduksi) parsial pada tekanan dan suhu kamar.
BalasHapusDapat di lihat :
1. Benzena di katalis dengan Na CH3COOH dan kalor tidak terjadi reaksi.
2. Naftalen di reaksikan dengan Na CH3COOH dan kalor menghasilkan tetralin.
3. Antrasena di reaksikan dengan bantuan katalis Na CH3COOH dan kalor menghasilkan 9,10- dihidroantrasena .
reaksi tersebut monosiklik seperti benzena, bisiklik seperti naftalena, ataupun polisiklik seperti antrasena.
Perhatikan bahwa sistem cincin yang tereduksi parsial masih mengandung cincin benzena. Sebagian besar sifat aromatik dari sistem cincin masih ada dan dipertahankan.
Untuk menghidrogenasi semua cincin aromatik dalam naftalena dapat dilakukan pada suhu dan tekanan tinggi. Persamaan reaksinya :
Naftalen + 5H2 di reaksikan dengan( suhu 225 C 35 atm ) pt menghasilkan dekalin.
baiklah raudhah, saya akan menjawab sepehamannya saya.
BalasHapusreaksi reduksi itu dpat dikatakan juga reaksi hidrogenasi dimana senyawa aromatik, yaitu naftalena direaksikan dengan H2. H2 disini jika kita tinjau dia adalah suatu elektrofilik jd hodrogen ini akan berikatan dengan naftalen yg memiliki ikatan pi (ikatan rangkapnya) karena disana byk terdapat elektron. Dikatakan parsial maksudnya sebagian, jd tidak semua ikatan rangkap pada naftalen diikatn oleh hidrogen karena naftalen masih bersifat aromatik dimana ikatannya stabil dan terjadi suatu persebaran elektron yg merata dan terus menerus.
Jadi reduksi parsial pada naftalen tergantung pada berapa banyak H2 yg dibutuhkan, dan stlh naftalen berikatan dgn hidrogen maka ikatan rangkapnya akan menjadi tunggal.
begitu kira-kira
Menurut saya, Reduksi pada naftalena dalam produk-produk reduksi yang berlangsung secara parsial tersebut sebagian karakter aromatis sistem cincin masih dipertahankan. Misalnya Naftalen di reaksikan dengan Na CH3COOH dalam kondisi panas (kalor) menghasilkan tetralin. Reduksi naftalena pada kondisi berbeda terjadi bila reduksi berlangsung secara total (lengkap) dimana seluruh ikatan rangkap pada senyawa polisiklis aromatis tersebut tereduksi. Untuk dapat berlangsungnya reduksi total tentu diperlukan kalor dan tekanan yang tinggi. Kondisi reaksi yang berat tersebut diperlukan untuk mengatasi kehilangan sifat aromatis pada produk reduksi. Yang mana dapat dilakukan dengan cara naftalena direduksi oleh hidrogen menggunakan katalis platina pada tekanan 225oC, tekanan 35 atm. Semoga dapat membantu..
BalasHapusreaksi subtitusi antrasena dan fenantrena??????????????????
BalasHapus